Tumore al polmone ALK
Inibitori di ALK e generazioni farmacologiche
1. Razionale molecolare degli inibitori tirosin-chinasici di ALK
L’identificazione delle fusioni geniche coinvolgenti ALK ha consentito lo sviluppo di inibitori tirosin-chinasici (TKI) selettivi, capaci di bloccare l’attività chinasica costitutivamente attiva della proteina di fusione.
Gli inibitori di ALK si legano al sito catalitico ATP-dipendente della tirosin-chinasi, impedendo la fosforilazione dei substrati intracellulari e determinando l’inibizione delle principali vie di segnalazione proliferativa e anti-apoptotica, tra cui:
• PI3K–AKT–mTOR
• MAPK–ERK
• JAK–STAT
Questo blocco molecolare induce:
• arresto del ciclo cellulare
• riduzione della proliferazione
• aumento dell’apoptosi
• riduzione della capacità metastatica
2. Evoluzione farmacologica degli inibitori di ALK
Lo sviluppo degli inibitori di ALK ha seguito una progressione generazionale, guidata principalmente dall’emergere dei meccanismi di resistenza acquisita e dalla necessità di migliorare la penetrazione cerebrale.
2.1 Prima generazione: crizotinib
Crizotinib è stato il primo inibitore di ALK approvato per il trattamento del NSCLC ALK-positivo.
Caratteristiche principali:
• attività anti-ALK e anti-MET
• elevata efficacia sistemica iniziale
• scarsa penetrazione della barriera emato-encefalica
Limiti clinici:
• sviluppo precoce di resistenza (mediana PFS ≈ 10–12 mesi)
• elevata incidenza di progressione cerebrale
2.2 Seconda generazione: alectinib, brigatinib, ceritinib
Questi farmaci sono stati sviluppati per superare le principali mutazioni di resistenza emerse sotto crizotinib.
Vantaggi principali:
• maggiore affinità per il dominio chinasico di ALK
• miglior profilo di selettività
• eccellente penetrazione cerebrale
• capacità di inibire numerose mutazioni secondarie
Alectinib e brigatinib rappresentano attualmente lo standard terapeutico di prima linea, garantendo:
• PFS mediana > 30 mesi
• elevato controllo intracranico
• miglior tollerabilità
2.3 Terza generazione: lorlatinib
Lorlatinib è stato progettato specificamente per superare mutazioni complesse di resistenza, in particolare la mutazione G1202R.
Caratteristiche farmacologiche distintive:
• struttura macro ciclica altamente flessibile
• potente attività contro la maggior parte delle mutazioni note
• eccellente attraversamento della barriera emato-encefalica
Lorlatinib rappresenta oggi il farmaco con lo spettro d’azione più ampio contro ALK, particolarmente indicato nelle sequenze terapeutiche avanzate.
3. Meccanismi molecolari di resistenza agli inibitori di ALK
Nonostante l’elevata efficacia iniziale, quasi tutti i pazienti sviluppano resistenza acquisita entro un periodo variabile.
I meccanismi di resistenza si suddividono in:
• meccanismi ALK-dipendenti
• meccanismi ALK-indipendenti
3.1 Resistenze ALK-dipendenti
Sono dovute all’insorgenza di mutazioni puntiformi nel dominio tirosin-chinasico, che alterano la conformazione della proteina impedendo il legame del farmaco.
Le mutazioni più rilevanti includono:
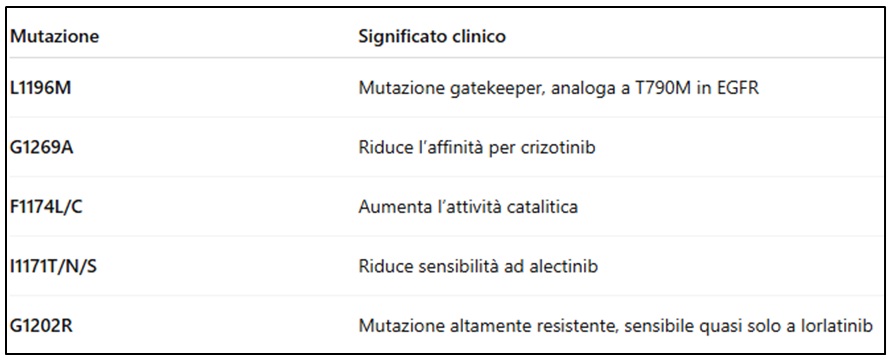
La mutazione G1202R rappresenta la principale causa di fallimento dei TKI di seconda generazione.
3.2 Resistenze ALK-indipendenti (bypass signaling)
In circa il 30–40% dei casi, la resistenza non coinvolge direttamente ALK, ma l’attivazione di vie di segnalazione alternative, tra cui:
• amplificazione di MET
• attivazione di EGFR
• mutazioni di KRAS
• attivazione delle vie PI3K–AKT e MAPK
Questi meccanismi permettono alla cellula tumorale di aggirare il blocco di ALK, mantenendo attiva la proliferazione.
3.3 Resistenza fenotipica
In alcuni casi si osserva una trasformazione istologica:
• transizione epitelio-mesenchimale (EMT)
• trasformazione in carcinoma a piccole cellule
Queste forme di resistenza sono associate a prognosi peggiore e minore sensibilità ai TKI (Riassunto Fig.1).
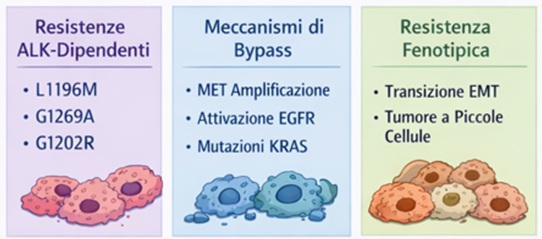
Fig 1. Meccanismo di resistenza agli inibitori ALK
4. Monitoraggio molecolare dinamico e biopsia liquida
La biopsia liquida, mediante analisi del DNA tumorale circolante (ctDNA), consente di:
• identificare precocemente mutazioni di resistenza
• monitorare l’evoluzione clonale del tumore
• guidare in tempo reale le decisioni terapeutiche
Questa strategia permette una medicina di precisione adattativa, in cui la terapia viene modulata sulla base del profilo mutazionale emergente.
5. Strategie terapeutiche per il superamento della resistenza
L’approccio moderno prevede una sequenza razionale dei TKI, basata sul meccanismo molecolare di resistenza:
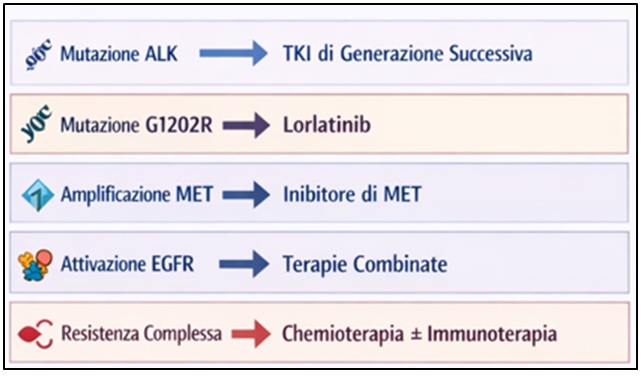
Le strategie combinate rappresentano oggi un importante filone di ricerca clinica.
6. Resistenze complesse post-lorlatinib
Dopo lorlatinib emergono mutazioni compound, cioè combinazioni multiple di mutazioni nello stesso allele, che generano conformazioni proteiche estremamente resistenti.
Questo scenario rappresenta la nuova frontiera terapeutica, per la quale sono in sviluppo:
• inibitori di quarta generazione
• terapie bispecifiche
• strategie multi-target
Conclusione
L’evoluzione degli inibitori di ALK rappresenta uno dei migliori esempi di oncologia di precisione dinamica, in cui il trattamento viene costantemente adattato all’evoluzione molecolare del tumore.
La comprensione dei meccanismi di resistenza ha permesso:
• lo sviluppo di farmaci sempre più potenti
• una sequenza terapeutica razionale
• un significativo prolungamento della sopravvivenza
Nei pazienti ALK-positivi, la malattia può oggi essere controllata per molti anni, trasformandosi progressivamente in una condizione cronica molecolarmente gestibile.

Dott. ssa Jessica Evangelista
Policlinico Universitario Agostino Gemelli – Roma