KRAS e immunoterapia nel tumore del polmone
Microambiente tumorale, infiammazione e perché alcuni tumori rispondono meglio
Introduzione: perché parlare di KRAS oggi
Negli ultimi anni, la comprensione del tumore del polmone non è più basata solo su “dove nasce il tumore” o “quanto è grande”, ma soprattutto sulle sue caratteristiche molecolari. Tra queste, una delle più importanti è la mutazione del gene KRAS, presente in circa il 25–30% degli adenocarcinomi polmonari.
Per molti anni KRAS è stato considerato un bersaglio “difficile” da trattare. Oggi, invece, sappiamo che non solo esistono terapie mirate per alcune sue varianti (come KRAS G12C), ma soprattutto che KRAS influenza profondamente la risposta all’immunoterapia.
Questo articolo esplora un aspetto fondamentale e spesso poco spiegato ai pazienti: non è solo la mutazione in sé a contare, ma l’ambiente che essa crea attorno al tumore.
1. Il microambiente tumorale: il “quartiere” del tumore
Per capire KRAS e immunoterapia, bisogna immaginare il tumore non come una massa isolata, ma come una città viva.
- Le cellule tumorali sono le “case”
- I vasi sanguigni sono le “strade”
- Le cellule immunitarie sono la “polizia e l’esercito”
- Le molecole infiammatorie sono i “segnali di allarme”
Tutto questo insieme si chiama microambiente tumorale.
KRAS e microambiente
Quando KRAS è mutato, la cellula tumorale non cresce solo più velocemente, ma cambia anche il modo in cui “dialoga” con il sistema immunitario.
In particolare può:
- attirare cellule infiammatorie “sbagliate”
- ridurre l’attività dei linfociti T (le cellule che uccidono il tumore)
- aumentare segnali che “spengono” il sistema immunitario
2. Infiammazione: un’arma a doppio taglio
L’infiammazione è un elemento centrale nel tumore del polmone.
In condizioni normali, l’infiammazione serve a:
• eliminare infezioni
• riparare i tessuti
Nel tumore, però, può diventare cronica e favorire la crescita tumorale.
KRAS e infiammazione
Le mutazioni di KRAS possono attivare vie molecolari (come MAPK e NF-κB) che:
• aumentano la produzione di citochine infiammatorie
• creano un ambiente “fertile” per il tumore
• riducono l’efficacia delle cellule immunitarie
Questo porta a un paradosso:
⇒ più infiammazione non significa sempre più difesa immunitaria
⇒ a volte significa più supporto al tumore
3. TMB e PD-L1: i due indicatori chiave dell’immunoterapia
Quando si parla di immunoterapia nel tumore del polmone, due parametri sono fondamentali:
• TMB (Tumor Mutational Burden)
• PD-L1 (Programmed Death-Ligand 1)
3.1 TMB: il “numero di errori” del tumore
Il TMB misura quante mutazioni ha il DNA del tumore.
• TMB alto → molte mutazioni → tumore più “visibile” al sistema immunitario
• TMB basso → tumore più “nascosto”
Perché è importante
Più mutazioni significano più “etichette strane” sulla cellula tumorale, che il sistema immunitario può riconoscere.
3.2 PD-L1: il “freno” del sistema immunitario
PD-L1 è una proteina che il tumore usa per spegnere i linfociti T.
Quando PD-L1 è alto:
• il tumore “disattiva” i linfociti
• l’immunoterapia (anti-PD-1 / anti-PD-L1) può riattivarli
Esempio per pazienti
Immaginiamo i linfociti T come soldati:
• PD-L1 è un “segnale falso” che dice ai soldati: non attaccare, è tutto normale
• l’immunoterapia toglie questo segnale e permette ai soldati di combattere
4. Perché alcuni tumori KRAS-mutati rispondono meglio all’immunoterapia
Non tutti i tumori KRAS-mutati sono uguali. Alcuni rispondono molto bene all’immunoterapia, altri meno.
Questo dipende da una combinazione di fattori:
4.1 KRAS non è “da solo”
La risposta immunitaria dipende da co-mutazioni importanti, per esempio:
• STK11/LKB1 → spesso associata a scarsa risposta immunitaria
• TP53 → spesso associata a maggiore infiammazione e migliore risposta
• KEAP1 → spesso associata a resistenza
⇒ Quindi KRAS è solo “il primo livello”, ma il contesto genetico è decisivo.
4.2 KRAS + TP53: il profilo “caldo”
Quando KRAS è associato a mutazione di TP53:
• aumenta l’infiammazione
• aumenta il TMB
• il tumore diventa più “visibile”
⇒ Questi tumori spesso rispondono meglio all’immunoterapia
4.3 KRAS + STK11: il profilo “freddo”
Quando KRAS è associato a STK11:
- il microambiente è povero di linfociti T
- bassa infiammazione “utile”
- scarsa risposta a immunoterapia
⇒ Anche se PD-L1 può essere presente, la risposta è spesso limitata
4.4 Il ruolo del microambiente immunitario
Oltre ai geni, conta anche la presenza reale di cellule immunitarie nel tumore:
- “hot tumor” → ricco di linfociti → migliore risposta
- “cold tumor” → povero di linfociti → risposta ridotta
KRAS può influenzare questa distribuzione, ma non in modo uniforme.
Conclusione: verso una medicina sempre più personalizzata
Oggi non possiamo più dire semplicemente:
“KRAS positivo = risposta o non risposta all’immunoterapia”
La realtà è molto più complessa e interessante.
La risposta dipende da:
- microambiente tumorale
- livello di infiammazione
- TMB
- PD-L1
- co-mutazioni genetiche
- presenza di linfociti nel tumore
Messaggio chiave per i pazienti
L’immunoterapia non è una terapia “uguale per tutti”, ma una strategia che funziona meglio quando:
- il tumore è riconoscibile dal sistema immunitario
- il microambiente non lo protegge troppo
- il sistema immunitario è già “parzialmente attivo”
Prospettive future
La ricerca su KRAS sta andando verso:
- combinazioni tra immunoterapia e terapie mirate (es. KRAS G12C inhibitors)
- modulazione del microambiente tumorale
- biomarcatori più precisi del solo PD-L1
L’obiettivo è chiaro:
⇒ capire non solo se un tumore risponderà, ma perché risponderà.
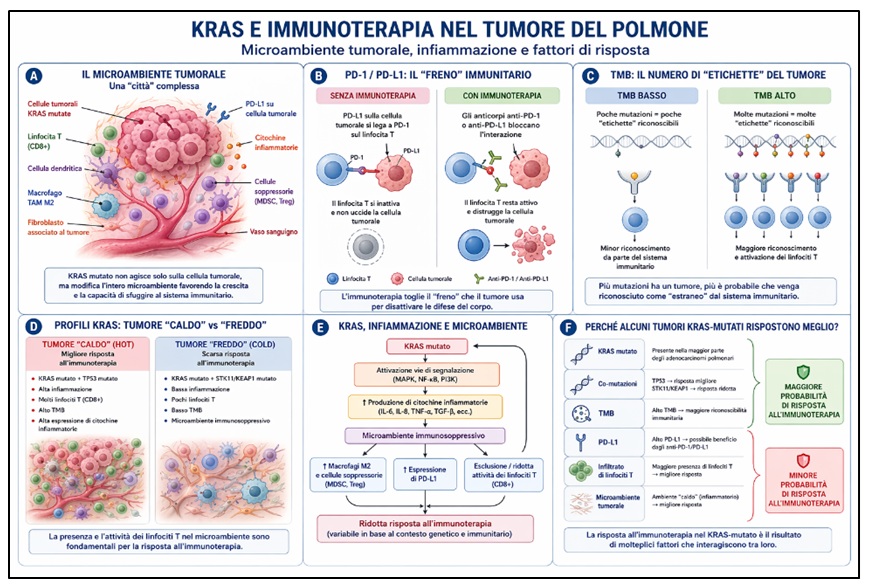
Immagine riassuntiva KRAS e IMMUNOTERAPIA NEL TUMORE DEL POLMONE

Dott. ssa Jessica Evangelista
Policlinico Universitario Agostino Gemelli – Roma
Quesito posto il 17/04/2026
Gentile dottoressa,
sono affetto da carcinoma polmonare non a piccole cellule, squamoso con PDL1 pari al 70%; dopo un primo trattamento con immunoterapia, al primo controllo Tac è emersa una progressione.
Dal precedente esame molecolare era emersa una sola mutazione G12X, quindi non G12C, ma non meglio identificata dal laboratorio.
La mia domanda riguarda informazioni aggiornate circa la possibilità del laboratorio di identificare gli altri sottoposti, la possibile interferenza di tale mutazione sull’esito della prima Tac, e se sono ipotizzabili nuovi trattamenti per altri sottotipi di tale mutazione .
La ringrazio di cuore.
Pietro
Gentile sig. Pietro,
la mutazione riscontrata (KRAS G12X) indica un’alterazione a carico del gene KRAS a livello del codone 12, ma senza una specificazione del singolo amminoacido coinvolto (ad esempio G12A, G12D, G12V, G12R, ecc.).
La maggior parte dei laboratori di biologia molecolare oggi è in grado di raffinare ulteriormente la tipizzazione di queste varianti. In particolare, è possibile utilizzare pannelli NGS (Next Generation Sequencing) multigene di nuova generazione, che rappresentano lo standard attuale per l’analisi molecolare, in quanto consentono una lettura più completa e sensibile delle alterazioni genetiche. In alternativa, in casi selezionati, possono essere impiegati metodi mirati come PCR allelica o digital PCR, che permettono la ricerca specifica di varianti note. Tuttavia, l’NGS rimane la metodica di riferimento per ottenere una caratterizzazione più ampia e accurata.
Nel caso in cui l’analisi precedente sia stata eseguita con pannelli più limitati o con una copertura non ottimale del gene KRAS, è possibile che la variante non sia stata ulteriormente discriminata nel dettaglio. Per questo motivo, un eventuale approfondimento con metodiche più aggiornate o su nuova piattaforma può consentire una migliore definizione del sottotipo mutazionale, a condizione che il materiale biologico disponibile sia adeguato oppure che sia possibile l’analisi su DNA circolante (biopsia liquida) con sufficiente qualità e quantità.
Per quanto riguarda l’andamento alla TC dopo immunoterapia, la presenza di questa mutazione non determina di per sé l’esito della risposta radiologica, che dipende da molteplici fattori clinici e biologici da valutare nel loro insieme.
Al momento, per le varianti di KRAS diverse da G12C non sono disponibili terapie target specifiche approvate, e le eventuali opzioni terapeutiche dipendono dal quadro clinico complessivo e dalle linee di trattamento disponibili.
Per qualsiasi dubbio di natura strettamente clinica o terapeutica, è comunque fondamentale fare riferimento all’oncologo di riferimento, che potrà inquadrare il caso nel percorso di cura più appropriato.
Cordialmente

Dott. ssa Jessica Evangelista
Policlinico Universitario Agostino Gemelli – Roma