Mutazioni di EGFR: canoniche e non canoniche
Mutazioni di EGFR: quando il segnale cambia forma
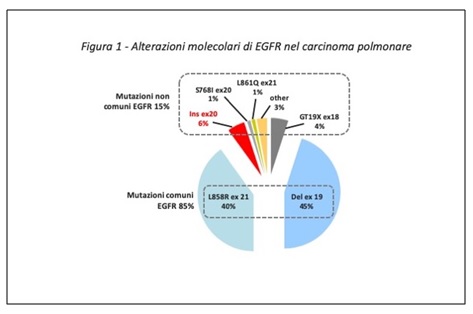
Dopo aver compreso il ruolo fisiologico di EGFR e il suo comportamento anomalo nella cellula tumorale, il passo successivo è capire come questo recettore si altera. Non tutte le mutazioni di EGFR sono uguali: alcune sono molto comuni e ben conosciute, altre sono più rare e complesse. Questa distinzione è oggi fondamentale perché influenza direttamente le scelte terapeutiche (vedi Figura 1).
Nel carcinoma polmonare non a piccole cellule (NSCLC), le mutazioni di EGFR interessano principalmente il dominio tirosin-chinasico del recettore, la parte responsabile della trasmissione del segnale di crescita all’interno della cellula.
Mutazioni canoniche di EGFR: le più frequenti e studiate
Con il termine mutazioni canoniche si indicano le alterazioni di EGFR più comuni, quelle che rappresentano circa l’85–90% di tutte le mutazioni di EGFR nel NSCLC. Sono definite “classiche” perché sono state le prime ad essere identificate e le più studiate dal punto di vista biologico e clinico (1).
Le due principali mutazioni canoniche sono:
• Delezione dell’esone 19: consiste nella perdita di una piccola porzione di DNA che altera la struttura del recettore;
• Mutazione L858R dell’esone 21: una singola sostituzione aminoacidica che rende EGFR costitutivamente attivo.
Dal punto di vista biologico, entrambe le mutazioni determinano un’attivazione continua del recettore, indipendente dal legame con il ligando. Il segnale di crescita rimane quindi sempre acceso, favorendo proliferazione e sopravvivenza cellulare.
Queste mutazioni spiegano perché molti pazienti con tumore EGFR-mutato rispondano in modo così marcato agli inibitori tirosin-chinasici (TKI): il farmaco blocca proprio il meccanismo centrale da cui il tumore dipende (2).
Perché le mutazioni canoniche rispondono bene alle terapie mirate
Le mutazioni canoniche modificano la struttura della tasca catalitica di EGFR, rendendola particolarmente sensibile al legame con i TKI. In altre parole, il farmaco “entra” facilmente nel recettore mutato e ne spegne l’attività.
Questo spiega perché, nei pazienti con delezione dell’esone 19 o mutazione L858R, i TKI di prima, seconda e terza generazione abbiano dimostrato:
• elevati tassi di risposta;
• rapido controllo della malattia;
• miglioramento significativo della qualità di vita rispetto alla chemioterapia tradizionale.
Dal punto di vista del paziente, questo si traduce spesso in terapie orali, meglio tollerate e più mirate, con un impatto importante sulla quotidianità (3).
Mutazioni non canoniche di EGFR: un gruppo eterogeneo
Accanto alle mutazioni canoniche esiste un gruppo più ampio e complesso di alterazioni definite mutazioni non canoniche. Queste rappresentano circa il 10–15% delle mutazioni di EGFR e includono modifiche genetiche molto diverse tra loro (4).
Tra le principali mutazioni non canoniche troviamo:
• Mutazioni dell’esone 18;
• Inserzioni dell’esone 20;
• Mutazioni rare dell’esone 21 diverse da L858R;
• Mutazioni complesse, in cui sono presenti più alterazioni contemporaneamente.
A differenza delle mutazioni canoniche, queste alterazioni non producono tutte lo stesso effetto biologico. Alcune attivano EGFR in modo simile alle forme classiche, altre modificano il recettore in modo più sottile o alterano la sua sensibilità ai farmaci.
Inserzioni dell’esone 20: perché sono diverse
Le inserzioni dell’esone 20 meritano un’attenzione particolare. In queste mutazioni, piccoli frammenti di DNA vengono inseriti nel gene EGFR, causando un cambiamento strutturale che rende il recettore attivo ma poco accessibile ai TKI tradizionali (5).
Dal punto di vista clinico, questo significa che molti dei farmaci efficaci nelle mutazioni canoniche risultano meno attivi o inefficaci nelle inserzioni dell’esone 20.
Questa differenza biologica ha rappresentato per anni una sfida terapeutica, ma ha anche stimolato lo sviluppo di nuovi farmaci specificamente progettati per queste alterazioni.
Mutazioni rare e risposta variabile ai trattamenti
Non tutte le mutazioni non canoniche si comportano allo stesso modo. Alcune mutazioni dell’esone 18, ad esempio, possono rispondere bene a determinati TKI, mentre altre mostrano una sensibilità intermedia (6).
Questo rende evidente un concetto chiave: non è sufficiente sapere che EGFR è mutato, è essenziale sapere quale mutazione è presente.
Dal punto di vista del paziente, questo sottolinea l’importanza della caratterizzazione molecolare accurata del tumore, attraverso test genetici sempre più sofisticati.
Implicazioni cliniche: dalla biologia alla terapia personalizzata
La distinzione tra mutazioni canoniche e non canoniche non è solo una classificazione accademica, ma ha conseguenze dirette sulla scelta del trattamento.
• Le mutazioni canoniche sono oggi un esempio emblematico di successo della medicina di precisione.
• Le mutazioni non canoniche richiedono un approccio più personalizzato, spesso basato su evidenze emergenti e su farmaci di nuova generazione.
Questo approccio “su misura” rappresenta uno dei cambiamenti più profondi dell’oncologia moderna.
Messaggio chiave
Le mutazioni di EGFR non sono tutte uguali. Capire la differenza tra forme canoniche e non canoniche significa comprendere perché alcuni pazienti rispondono molto bene alle terapie mirate e altri necessitano di strategie diverse.
Nel tumore del polmone, la conoscenza dettagliata della mutazione non è un dettaglio tecnico: è il punto di partenza per una cura davvero personalizzata.
Bibliografia:
1. Shigematsu H, Gazdar AF. Somatic mutations of epidermal growth factor receptor signaling pathway in lung cancers. Int J Cancer. 2006;118(2):257–262.
2. Lynch TJ et al. Activating mutations in the epidermal growth factor receptor underlying responsiveness of non–small-cell lung cancer to gefitinib. N Engl J Med. 2004;350(21):2129–2139.
3. Paez JG et al. EGFR mutations in lung cancer: correlation with clinical response to gefitinib therapy. Science. 2004;304(5676):1497–1500.
4. Shigematsu H, Gazdar AF. Somatic mutations of epidermal growth factor receptor signaling pathway in lung cancers. Int J Cancer. 2006;118(2):257–262.
5. Yasuda H et al. Structural, biochemical, and clinical characterization of epidermal growth factor receptor (EGFR) exon 20 insertion mutations in lung cancer. Sci Transl Med. 2013;5(216):216ra177.
6. Beau-Faller M et al.Rare EGFR exon 18 and exon 20 mutations in non–small-cell lung cancer: clinical and molecular characteristics. J Clin Oncol. 2014;32(25):2720–2726.

Dott. ssa Jessica Evangelista
Policlinico Universitario Agostino Gemelli – Roma