CERITINIB
Primo inserimento: 20/06/2016; ultimo aggiornamento: luglio 2022
Nome commerciale
Zykadia ®
Compagnia farmaceutica produttrice
Sviluppato e commercializzato dalla Novartis.
Indicazione approvata dal SSN
Ceritinib è indicato per il trattamento dei pazienti adulti con carcinoma
polmonare non a piccole cellule (NSCLC) che sia positivo per la chinasi del linfoma anaplastico (ALK), in prima linea o dopo Crizotinib. Per maggiori info, si rimanda al documento AIFA del 10/5/2018.
Caratteristiche chimico-farmacologiche
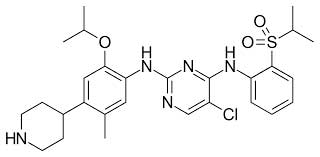
E’ una piccola molecola (peso molecolare 558,14 g/ml).
La sua formula chimica è: C28H36N5O3S. Nome chimico: 2,4-Pirimidindiamina, 5-cloro-N4-[2-[(1-metilletil)sulfonil]fenil]-N2-[5-metil-2-(1-metiletossi)-4-(4-piperidinil)fenil].
Meccanismo d’azione
Ceritinib è un potente inibitore ALK (ovvero agisce su tumori che presentano variazioni dell’enzima chiansi del linfoma anaplastico, come la traslocazione EML4-ALK) ed è efficace anche a sopraggiunta resistenza al Crizotinib.
Modalità di somministrazione
Uso orale. La dose raccomandata è di 450 mg assunta per via orale una volta al giorno, col cibo e sempre alla stessa ora. Per maggiori informazioni si rimanda alla scheda tecnica dell’EMA europea.
Attività antitumorale riconosciuta
Oggi, il farmaco è uno standard terapeutico per il NSCLC (vedi su), ma tutto nasce da uno studio di fase I presentato all’ASCO meeting del 2013 (Shaw A, et al. Abstract n. 8010) in cui era stata osservata una “fenomenale” attività anti-tumorale in tumori non a piccole cellule del polmone (NSCLC) ALK-positivi, con risposte obiettive del 59-62%, anche in pazienti pre-trattati con Crizotinib.
Attività antitumorale (cancro al polmone)
Vedi su.
Indicazioni cliniche
Come riconosciuto dalle principali agenzie governative del farmaco, inclusa la nostra AIFA, l’indicazione è quella del NSCLC inoperabile (localmente avanzato o metastatico) con mutazione ALK, anche dopo trattamento di prima linea con Crizotinib. La rara mutazione del gene ROS1 è un’altra forte indicazione al trattamento con inibitori-ALK, Ceritinib incluso. Attualmente (1/7/22), 1 solo studio clinico è in corso -ed attivamente arruolante pazienti- sul Ceritinib (censimento NIH). Nella letteratura medica mondiale, alla stessa data, sono però 100 i lavori conclusi e pubblicati che riguardano il Ceritinib nel cancro del polmone (vai alla pagina). Fra questi ultimi, suggeriamo di visionare l’ultimo aggiornamento dei dati dello studio ASCEND-1 e quelli, più recenti dello studio ASCEND-4.
Effetti tossici e collaterali
Gli effetti collaterali più comuni sono stati nausea, vomito, e diarrea. Ve ne sono altri, come l’elevazione degli enzimi epatici, che si presentano meno frequentemente. La tossicità è ampiamente discussa in questo documento in lingua italiana della European Medicines Agency (EMA).
Nostri articoli
//
Altre letture consigliate
FARMACI MIRATI

